■ 核心亮点:
✪ 深圳泛因医学有限公司是一家致力于开发高通量读写T和B淋巴细胞受体谱关键技术及其在临床检测和治疗方面应用的高科技创新企业,对标美国免疫医学诊断的明星项目Adaptive(NASDAQ:ADPT),聚焦极具潜力的肿瘤免疫治疗及MRD检测。由国际知名免疫学专家领衔,拥有临床级免疫组数据解码平台、完善的免疫组技术平台、以及先进的自研信息分析平台等技术优势,并拥有国内最大的临床免疫组数据库。
✪ 目前,泛因医学已启动Pre-A轮融资,凯乘资本担任财务顾问。欢迎联系微信Gavinzou8 或者邮箱:info@winxcap.com。
近日,深圳泛因医学有限公司研制的基于高通量测序(NGS)平台的血液肿瘤微小残留病(MRD)检测产品NEO-MRDTM获得了欧盟CE准入资质。根据欧盟《体外诊断医疗器械指令》规定,该检测产品已具备欧盟市场的准入条件,这标志着泛因医学将助力全球血液肿瘤微小残留病事业的发展。



微小残留病(Minimal Residual Disease, MRD)是指恶性肿瘤经过治疗后体内残留的微量肿瘤细胞的状态,是肿瘤复发的根源。MRD的水平一般比较低,需要用敏感性和特异性都非常高的方法来进行检测。白血病、恶性淋巴瘤及多发性骨髓瘤是常见的血液肿瘤,MRD 是指上述血液肿瘤经过治疗缓解后,在体内残留的少量血液肿瘤细胞。准确的MRD检测是对患者进行个性化精准治疗的基础。
1. 预测临床结果及对病人的危险程度进行分层。在临床应用指南中,诱导缓解治疗早期、 诱导缓解治疗后及巩固治疗开始前的MRD水平是判定疾病危险程度的重要依据。
2. 指导治疗决策。在诱导缓解阶段需要根据疾病危险程度不同而采用不同强度的治疗方案,在诱导缓解后对MRD阴性的病人也可以降低后期治疗强度,以减少毒副作用。
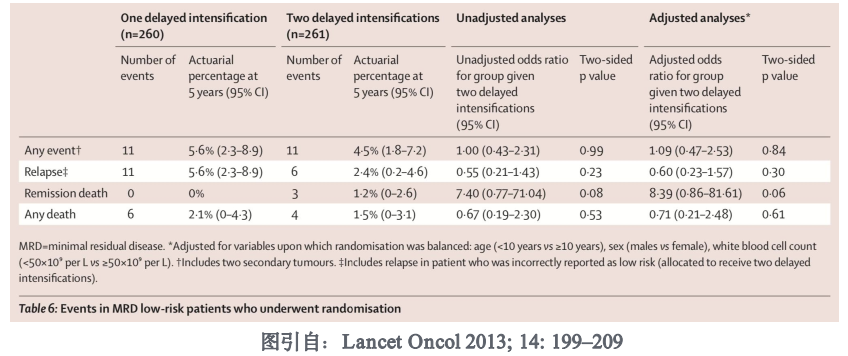
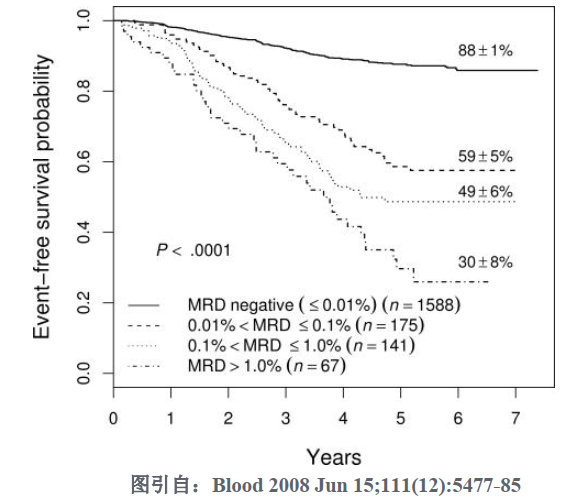
3. 早期预测肿瘤复发。诱导治疗后MRD阴性的病人的无病生存期显著高于 MRD 阳性的病人,MRD 阳性与疾病复发有直接关系。在急性淋巴白血病诊疗规范中,诱导缓解治疗早期(d15~19)MRD≥ 10-1,诱导缓解治疗后(d33~d45)MRD≥ 10-2,巩固治疗开始前(第 12 周左右)MRD≥ 10-4,都与不良预后相关。
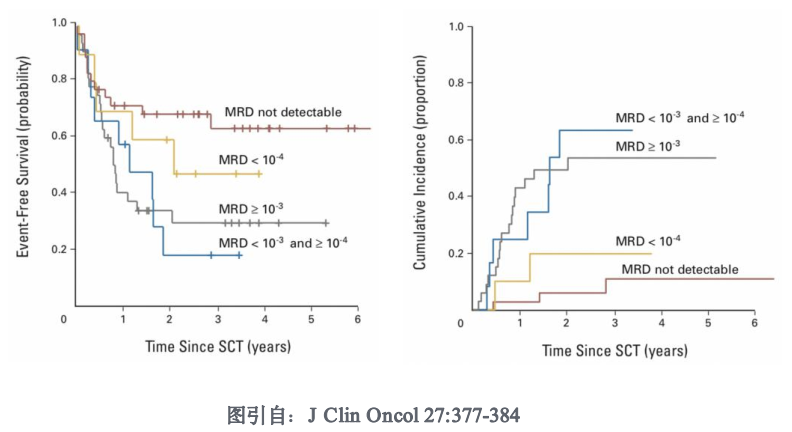
4. 确定骨髓或干细胞移植的最佳时间。移植前MRD水平与移植后病人的复发和长期生存有直接关系,移植前 MRD 水平越低,移植后复发的几率越小,EFS 越高。
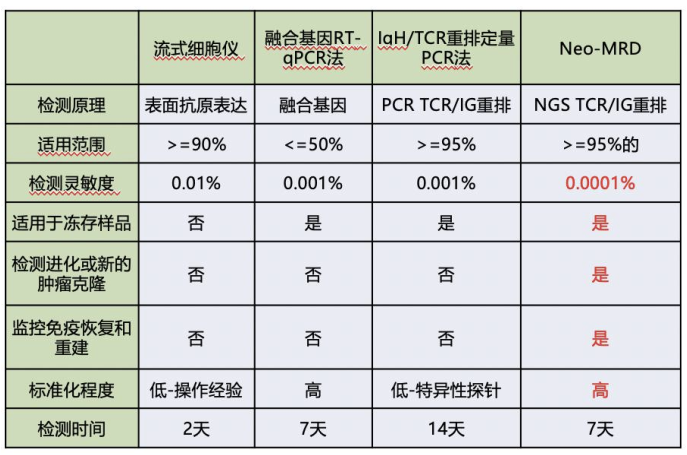
1.准确灵敏的实验系统。建立在无偏扩增系统上,准确性高,敏感性可以到 10-5-10-6,同时不受肿瘤细胞表面抗原漂移及克隆进化的影响。
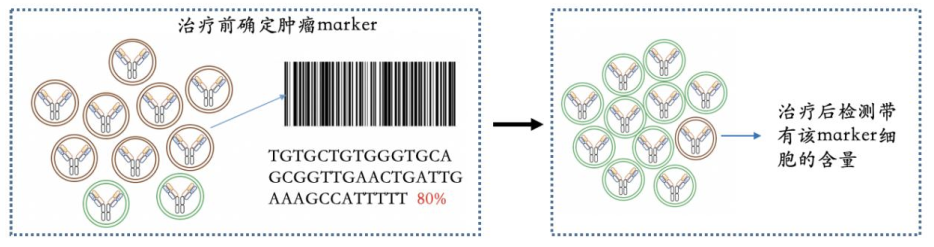
2.操作简便,流程标准化和自动化,减少人为操作误差。可以实现从DNA到检测报告的全自动化。重复性好。
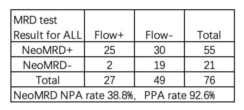
3.检出率高,通过扩增多条受体链提高肿瘤细胞的检出率。实验体系包括IGH、IGK、IGL、TRB、TRG的受体链,可以准确的鉴定肿瘤细胞的标志序列,同时每条链还包括不同位置(FR1、FR2、FR3)的引物,可以有效的避免由于肿瘤细胞的突变引起的假阴性或定量不准确。在58个真实临床样品检测中,NGS 和流式都阳性的25个样品两种方法的一致性较好,14 个样品流式阴性,NGS 阳性,19 个样品二者都阴性。
4.可以监测是否有新的高频克隆出现,评估由于原肿瘤亚克隆的亚克隆或演化克隆导致的复发风险。
5.对免疫系统的重建情况进行评估。
6.原创的生物信息分析工具。由于部分样品的MRD水平极低,需严格控制测序错误及序列污染。我们通过原创的数据处理技术可以有效的校正测序错误及去除实验过程可能出现的微量污染,保证检测的准确性。
泛因医学已经与多家企业和机构进行合作,推进血液瘤MRD检测项目的研发及应用,提高MRD检出率,提高患者的临床获益。泛因医学和全行业专家一起以科学的态度、不懈的努力和严谨的实践的精神推动行业发展,血液瘤MRD临床检测未来大有可为。

深圳泛因医学有限公司是一家致力于开发高通量读写T和B淋巴细胞受体谱关键技术及其在临床检测和治疗方面应用的高科技创新企业。2020年获得深圳创新创业大赛盐田赛区三等奖、深圳国际生物生命健康产业展览会创新成果奖。

